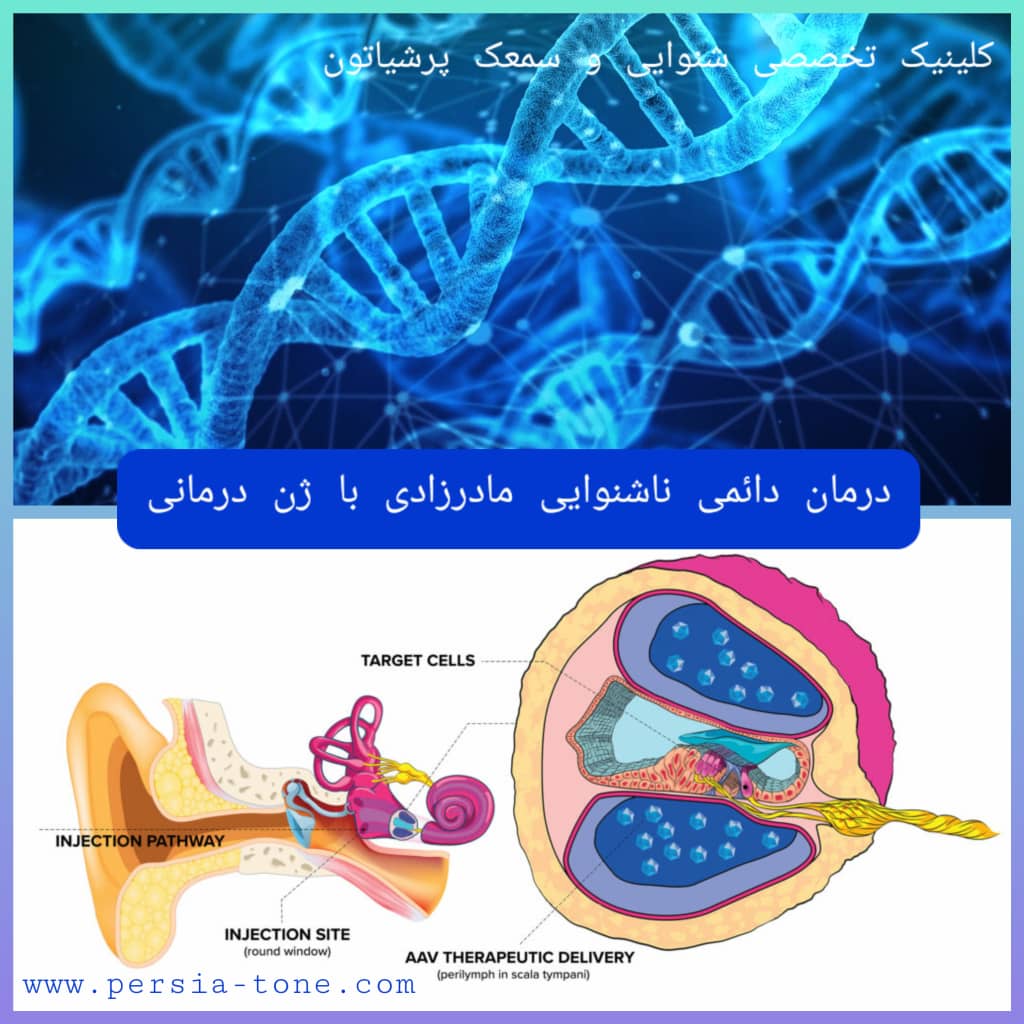
درمان دائمی ناشنوایی مادرزادی به کمک ژندرمانی
روش درمانی جدیدی برای درمان ناشنوایی مادرزادی ژنتیکی معرفی شده است که با انتقال ژن به سلولهای پوششی داخلی گوش میتواند عملکرد شنوایی را بهطور دائمی بازیابی کند. گروهی از پژوهشگران موفق شدند شنوایی را در موش دارای ناشنوایی DFNB9 (رایج ترین فرم ناشنوایی انسانی که ۸-۲ درصد از کل موارد نقایص ناشنوایی ژنتیکی مادرزادی را شامل میشود) بازیابی کنند. افراد دارای ناشنوایی DFNB9، بدلیل جهش ایجاد شده در ژن کد کنندهی اتوفرلین، (پروتئینی که نقشی کلیدی در انتقال اطلاعات صوتی در سیناپسهای سلولهای مویی گوش داخلی دارد.) عمیقا ناشنوا هستند، زیرا با وجود نبود نقایص قابل تشخیص در اپیتلیال حسی، این سیناپسها نمیتوانند در پاسخ به تحریک صوتی ناقل عصبی آزاد کنند، بنابراین موشهای DFNB9 مدل مناسبی برای آزمایش کارآیی ژندرمانی ویروسی بهشمار میروند.
بیش از نیمی از نقایص شنوایی مادرزادی غیرسندرمی، دارای یک علت ژنتیکی بوده و حدود ۸۰ درصد از این موارد ناشی از فرمهای اتوزومی مغلوب (DFNB) هستند. در حال حاضر، کاشت حلزون تنها گزینهی درمانی بازیابی شنوایی در این بیماران است.
دانشمندان با تزریق داخل حلزونی این ژن در یک موش بالغ دارای ناشنوایی DFNB9، بهطور موفقیتآمیزی عملکرد سیناپسی شنوایی و آستانههای شنوایی را به سطح نزدیک نرمال برگرداندند و مسیر جدیدی را برای آزمایشهای ژندرمانی آینده در بیماران دارای DFNB9 گشودند. نتایج مطالعات نشان میدهند که پنجرهی درمانی برای انتقال محلی ژن برای بیماران دارای ناشنوایی مادرزادی DFNB9 میتواند وسیعتر شود و امیدهایی را برای استفاده از این یافتهها برای درمان دیگر فرمهای ناشنوایی فراهم میکند.
وکتورهای AVV، از امیدبخشترین وکتورها برای ژندرمانی بیماریهای انسانی محسوب میشوند. ژندرمانی مبتنی بر AAV، گزینهی درمانی امیدوارکنندهای برای درمان ناشنوایی است اما کاربرد آن توسط یک پنجرهی درمانی باریک محدود میشود. در انسانها، توسعهی گوش داخلی در داخل رحم کامل میشود و شنوایی تقریبا در هفتهی بیستم بارداری ممکن میشود بر این اساس فرمهای ژنتیکی ناشنوایی مادرزادی در دورهی نوزادی تشخیص داده میشوند. پس باید در رویکردهای ژندرمانی در مدلهای حیوانی این مسئله مدنظر قرار گیرد و کارایی ژندرمانی پس از توسعهی کامل سیستم شنوایی ارزیابی شود.
قطعا تکمیل مراحل پژوهشی و کاربرد بالینی این مطالعات، راهکاری امیدبخش برای بیش از ۴۶۶ میلیون انسان با ضایعه شنوایی در سراسر جهان را به همراه خواهد داشت و به نظر میرسد، علاوه بر پژوهش های ژن درمانی که امید به درمان مشکلات شنوایی ژنتیکی را به همراه دارد، پژوهش های گسترده در حوزه کاربرد داروها و «فاکتورهای نوروتروفیک» برای بازسازی سیناپس های ریبونی، پیشگیری از کاهش نورونهای اولیه شنوایی و رشد مجدد فیبرهای شنوایی که سالهاست در دست مطالعه میباشد نیز بتواند راهکاری امیدبخش برای پیشگیری و درمان کم شنوایی های ناشی از نویز، پیرگوشی و دیگر بیماری های اکتسابی دستگاه شنوایی باشد و بتوان به آینده درمان قطعی کاهش شنوایی های مادرزادی و اکتسابی، خوش بین بود.
گرچه توجه و تاکید به این حقیقت در مشاوره بیماران و مددجویان، که تمامی این مطالعات هنوز در مراحل پایانی پژوهشی هستند و کارایی بالینی تایید شده در نمونه های انسانی به صورت وسیع، گزارش نشده است و همچنان راهکارهای جبرانی مانند استفاده از سمعک و کاشت حلزون، گزینه بالینی مورد تایید و استفاده در تمام دنیا میباشند، جهت پیشگیری از سردرگمی مددجویان و پیشگیری از تاخیر احتمالی در دریافت توانبخشی شنیداری، ضروری به نظر میرسد تا زمانیکه با تایید کاربرد بالینی-انسانی روش های ژن درمانی و دارودرمانی و تدوین گایدلاین های درمانی و توانبخشی جهانی، بتوانیم درمان قطعی کم شنوایی را به مراجعانمان نوید دهیم...